


Conheça os tratamentos oferecidos:
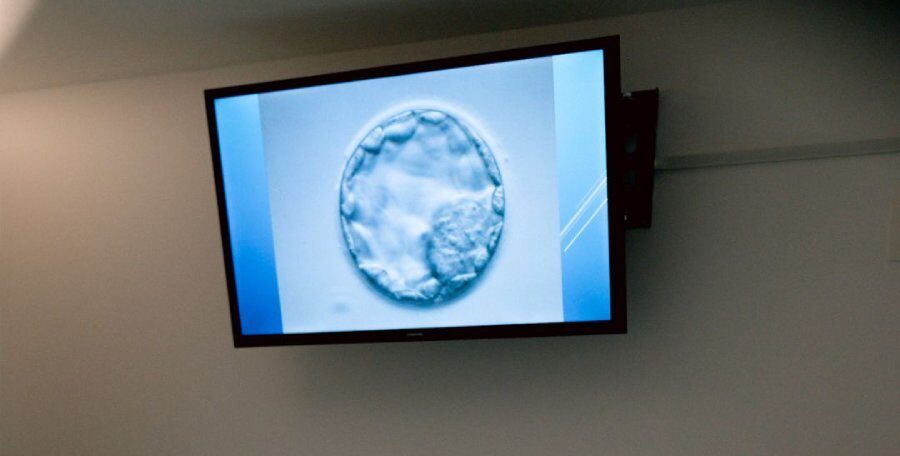
Hatching ou eclosão é termo usado para definir o momento no qual o embrião (produto da concepção entre o espermatozoide e o óvulo) rompe e deixa para trás a zona pelúcida, camada que o reveste, para que, posteriormente, se implante no endométrio (tecido que reveste o interior do útero) e a gestação seja alcançada.
No entanto, alguns embriões apresentam dificuldade neste processo de ruptura, sendo uma das causas de falhas na implantação. A assisted hatching, também conhecida apenas pela sigla “AH” ou “eclosão assistida” é uma técnica criada para auxiliar o embrião durante o processo de ruptura, facilitando a eclosão, e desta forma, é possível minimizar as falhas implantacionais por esse motivo.
A assisted hatching é um método de micromanipulação que abre um pequeno orifício na zona pelúcida momentos antes de o embrião ser transferido para o útero da paciente. Estudos científicos indicam que a eclosão assistida aumenta a taxa de implantação, bem como as chances de gravidez em determinados casos.
A técnica é indicada pelo médico ginecologista especializado em reprodução assistida, auxiliado pela equipe de embriologistas, e pode ser realizada de formas diferentes, como o método mecânico, método químico e o método laser (um dos mais utilizados atualmente).
Pacientes com idade avançada, mulheres com mais de 35 anos;
Falhas prévias na fertilização in vitro (FIV);
Pacientes em que os embriões apresentam a zona pelúcida espessa (grossa); Pacientes com diminuição da reserva ovariana (poucos óvulos);
Pacientes com endometriose;
Transferência de embriões criopreservados.
Além do assisted hatching (eclosão assistida), fazem parte das técnicas de alta complexidade: injeção Intracitoplasmática de espermatozoide (ICSI), injeção de espermatozoide morfologicamente selecionado (IMSI ou super ICSI), birrefringência da zona pelúcida, visualização do fuso meiótico, e diagnóstico genético pré implantacional (PGD/PGS), que são consideradas tecnologias e procedimentos complementares.
Os avanços médicos foram responsáveis por tornar os métodos de reprodução assistidas mais eficazes com o passar dos anos, e para acompanhar esse avanço o laboratório também se atualizou.
Atualmente, com equipamentos e meios de cultivo altamente específicos, o cultivo até blastocisto é uma estratégia de alguns laboratórios para aumentar as taxas de sucesso. O cultivo a blastocisto requer tecnologias de ponta e um embriologista em plena sintonia, pois todo o processo é importante, desde o meio até o tempo que o embrião é avaliado.
Ao atingir essa sintonia, o embriologista obtém blastocistos, que nada mais são do que embriões de alta qualidade, selecionados morfologicamente. A transferência de blastocistos garante melhores resultados, uma vez que são embriões em um estágio de desenvolvimento mais avançado.
Após a fertilização, o embrião começa seu processo de divisão, período no qual há aumento rápido no número de células que, passados alguns dias, compactam-se e formam um aglomerado de células (mórula). A partir do quinto dia, o estágio do embrião é chamado de blastocisto e já apresenta estrutura bem definida, além da formação de uma cavidade contendo líquido.
Em uma gravidez natural é o estágio em que o embrião está pronto para implantar no endométrio (camada que reveste internamente o útero da mulher) e a gravidez acontecer. No entanto, no caso das técnicas de reprodução humana, o embrião é formado em laboratório, ou seja, ele alcança o estágio blastocisto através dos estímulos artificiais, processo que é chamado de cultura de blastocisto, e tem duração de 5 a 6 dias.
Terminado o processo de cultivo embrionário, a etapa seguinte é a seleção e escolha dos melhores embriões, consequentemente, com maior potencial de gerar uma gravidez e, desta forma, realizar a transferência embrionária (transferência para o útero materno onde seguirá o desenvolvimento de modo natural).
Indicações:
A cultura de blastocisto foi de grande ajuda para elevar as taxas de sucesso dos métodos de reprodução assistida, sendo a fertilização em vitro (FIV) uma das principais técnicas beneficiadas. Além de permitir que o cultivo in vitro seja maior, o procedimento dá boas condições para a escolha dos embriões, abordagem que aumenta o sucesso e evita o risco de gestações múltiplas, por exemplo.
A fertilização in vitro, conhecida também como FIV ou bebê de proveta, é um tratamento de reprodução assistida que ajuda muitos casais a realizar o sonho de ter um filho. As altas taxas de sucesso da fertilização in vitro, que podem chegar até 60% já na primeira tentativa, é uma das razões da grande procura e recomendação do tratamento para casais ou pessoas que não conseguem engravidar…
O sonho da gravidez, sobretudo de ser mãe ou pai, é um direito de todos, portanto, deve ser respeitado sempre. Cada vez, casais homoafetivos procuram médicos e clínicas especializadas, pois a medicina de reprodução assistida permite que esse sonho seja realizado. Independente da orientação sexual, estado civil e outros fatores que não cabem julgamentos, os tratamentos de fertilidade visam promover a gravidez de filhos biológicos.
Após a avaliação médica e uma longa conversa com o ginecologista especialista em reprodução humana, necessária para que todos os processos e questionamentos sejam esclarecidos, é definido qual método será aplicado para gerar a gravidez. É importante ressaltar que cada caso é tratado individualmente, porém, as normas do Conselho Federal de Medicina, principalmente em relação à doação, precisam ser seguidas criteriosamente.
No caso dos casais de mulheres, o sêmen utilizado nos tratamentos não pode ser de familiares de nenhuma das parceiras. O processo é feito através da doação de sêmen, porém, a norma reforça que o doador não pode conhecer a identidade dos receptores, bem como os receptores não podem conhecer quem é o doador. Sendo assim, o anonimato é obrigatório.
Para os casais de homens, o processo é um pouco mais complexo, porém, é totalmente possível. Os procedimentos exigem mais critérios, pois além da doação dos óvulos, que deve ser de uma doadora desconhecida, será necessária a barriga solidária (útero de substituição), que neste caso pode ser uma parente próxima (até 4° grau: mãe, irmã, tia ou prima). No Brasil, a gestação solidária feita por mulheres que não são familiares próximas é proibida. Quando o casal não tem nenhuma parente que aceite ser barriga solidária, é possível solicitar ao Conselho Regional de Medicina a liberação para que uma conhecida seja a doadora do útero.
Quais são os tratamentos para casais homoafetivos?
Em relação às técnicas de tratamento, existem duas maneiras de realizar o sonho da maternidade ou paternidade dos casais homoafetivos: a fertilização in vitro (FIV) e a inseminação intrauterina (IIU), também conhecida como inseminação artificial.
A escolha do tratamento a ser realizado é exclusiva do casal. No entanto, é de extrema importância ter um profissional especialista para acompanhar essa decisão, que envolve tanto o desejo, quanto a saúde da pessoa que vai gestar o bebê. É fundamental que o casal conheça sobre os procedimentos e saiba quais etapas precisarão seguir.
Confira quais são as diferenças entre os tratamentos:
– Fertilização in vitro: neste método indicado para casais de mulheres, é possível ter uma gestação compartilhada, onde ambas participam do processo de fecundação e gestação, ou seja, há a possibilidade de ser usado o óvulo de uma das mulheres, e sua parceira irá gerar o bebê. O casal acompanha todos os passos dados para a realização do procedimento, bem como a doação do espermatozoide. No mais, a fertilização segue o protocolo normal.
– Inseminação artificial: nesta técnica também indicada para casais de mulheres, apenas uma das parceiras irá ceder o óvulo e se tornará gestante. É um procedimento mais simples que a FIV e envolve poucas fases. O espermatozoide também é doado, escolhido no banco de esperma, e irá de “encontro” ao óvulo, por meio de um cateter apropriado inserido na cavidade uterina.
– Fertilização in vitro com óvulos de doação e útero de substituição (barriga solidária): método indicado para casais de homens. O processo é caracterizado pela utilização de óvulos de doação anônima. Após captar os óvulos da doadora, eles serão fertilizados com os espermatozoides de um dos parceiros, portanto, será formado o embrião em laboratório. A etapa seguinte é transferir o embrião para o útero da parente próxima que será responsável pela barriga solidária.
A injeção intracitoplasmática de espermatozoide (ICSI) é um método de fecundação avançada que se tornou uma alternativa revolucionária, uma vez que oferece alta taxa de concepção para homens que inicialmente eram diagnosticados com infertilidade irreversível ou intratável.
Em resumo, a ICSI é definida como um aprimoramento da fertilização in vitro clássica, porém, é considerada um dos tratamentos de reprodução assistida.
O procedimento de injeção intracitoplasmática de espermatozoide (ICSI), como o nome já indica, consiste em injetar o espermatozoide selecionado diretamente em um óvulo maduro por meio de uma agulha extremamente fina, conduta guiada pelo embriologista com auxílio de microscópio. Após o período que varia de 17 a 21 horas, a fertilização é verificada, ou seja, se os embriões estão se desenvolvendo (clivagem) para que, posteriormente, os melhores sejam transferidos para o útero da da pessoa que vai gestar o bebê.
Como a ICSI é um processo feito via laboratório, a primeira etapa é a estimulação da produção dos gametas na mulher e no homem. A etapa seguinte é coletá-los e avaliá-los.
No caso dos homens, a análise tem o objetivo de certificar a presença de espermatozoides no sêmen, bem como selecionar os mais capacitados.
A injeção intracitoplasmática de espermatozoide é uma das soluções para casos de infertilidade masculina nas quais os outros métodos de tratamento exigem uma determinada quantidade de espermatozoides
Outras indicações da ICSI são:
– Causas de infertilidade masculina severas, obstrutiva ou não obstrutiva, como a vasectomia prévia, a oclusão inflamatória, a ausência congênita do ducto deferente e a insuficiência testicular, que levam a ausência de espermatozoides no ejaculado.
Além da injeção intracitoplasmática de espermatozoide (ICSI) fazem parte das técnicas de alta complexidade: injeção de espermatozoide morfologicamente selecionado (IMSI), birrefringência da zona pelúcida, visualização do fuso meiótico, assisted hatching (eclosão assistida) e diagnóstico genético pré implantacional (PGD/PGS), que são consideradas tecnologias e procedimentos complementares.
A injeção de espermatozoide morfologicamente selecionado (IMSI ou Super-ICSI) é um dos métodos mais novos e modernos da reprodução assistida, uma vez que tem o auxílio das imagens em alta resolução, recurso que permite uma seleção ainda mais apurada dos melhores espermatozoides para a potencial gravidez.
A técnica tem o mesmo objetivo e processo semelhante ao da ICSI convencional (injeção intracitoplasmática de espermatozoide), sendo definida como uma variante. No entanto, na versão clássica, existe um aumento de cerca de 400 vezes do tamanho do espermatozoide via microscópio. Já na Super-ICSI, o conjunto óptico oferece uma aproximação de 4.000 a 12.000 vezes.
Além da escolha mais cuidadosa, a aproximação aumentada permite ainda avaliar o espermatozoide morfologicamente, ou seja, é feita uma “vistoria” interna, como a procura de depressões no corpo celular que são fortes indícios de danos no DNA; e uma análise de sua estrutura (cabeça, pescoço e cauda), características que também influência na definição dos gametas mais adequados.
As principais indicações da super ICSI são:
– Fator masculino grave e/ou com falhas prévias na fertilização in vitro (FIV); – Quadros de falhas na implantação embrionária;
– Espermatozoides com alto índice de fragmentação do DNA;
– Ciclo de FIV com baixa qualidade embrionária, sendo a causa masculina; – Casos recorrentes de abortamento.
Além injeção de espermatozoide morfologicamente selecionado (IMSI ou super ICSI) fazem parte das técnicas de alta complexidade: injeção de espermatozoide morfologicamente
selecionado (IMSI), birrefringência da zona pelúcida, visualização do fuso meiótico, assisted hatching (eclosão assistida) e diagnóstico genético pré implantacional (PGD/PGS), que são consideradas tecnologias e procedimentos complementares.
A inseminação artificial, também conhecida como inseminação intrauterina (IIU), é um método de tratamento de reprodução assistida. Porém, a técnica é menos complexa quando comparada às demais. Por isso, muitas vezes a inseminação intrauterina é escolhida como a primeira opção (em combinação com a estimulação ovariana) para o tratamento da infertilidade.
O método consiste em depositar os gametas masculinos (espermatozoides) diretamente na cavidade uterina, ou seja, diretamente no útero. O processo de fertilização na inseminação artificial é realizado pelo próprio organismo, ou seja, a formação do embrião ocorre naturalmente a partir do encontro entre óvulo e espermatozoide. No entanto, é importante ressaltar que o sêmen é previamente preparado em laboratório para concentrar o maior número possível de espermatozoides saudáveis.
As principais indicações para a inseminação artificial são:
– Diminuição leve da contagem espermática;
– Diminuição da motilidade (movimentação) dos espermatozoides;
– Aumento do número de espermatozoides com formas anormais;
– Fator cervical;
– Muco cervical hostil;
– Infertilidade sem causa aparente ou inexplicada;
– Produção independente (maternidade solo planejada).
A inseminação artificial pode ser realizada com o sêmen do parceiro, mas em alguns casos existe a possibilidade da utilização do banco de sêmen de doador. Mesmo que uma técnica de baixa complexidade, o primeiro passo é a consulta com o médico ginecologista especialista em reprodução humana. Mesmo sendo uma técnica de baixa complexidade, o primeiro passo é a consulta com um médico ginecologista especialista em reprodução humana, que irá avaliar cada caso individualmente e indicar o tratamento mais adequado.
Diferença entre inseminação artificial e fertilização in vitro (FIV)
Ambos os tratamentos têm o objetivo de promover a gravidez em casos de infertilidade, mas a inseminação artificial é mais simples do que a fertilização in vitro (FIV). Ambos podem começar com o estímulo da produção de óvulos por meio de medicamentos, porém o modo de fecundação é diferente.
Na FIV, a fecundação (formação do embrião) é realizada em laboratório, pois nesse caso o organismo não consegue realizar o processo de forma independente. Já na inseminação artificial, o encontro entre óvulo e espermatozoide acontece naturalmente dentro do corpo da mulher.
A taxa de sucesso por ciclo da fertilização in vitro clássica (FIV) ou da injeção intracitoplasmática de espermatozoide (ICSI) costuma ser maior do que a da inseminação artificial. O custo por ciclo da inseminação artificial, por outro lado, é menor que o da FIV e da ICSI, o que possibilita um maior número de tentativas. Ainda assim, estatisticamente, a chance de concepção após duas tentativas de FIV ou ICSI costuma ser consideravelmente maior do que após três ou quatro ciclos de inseminação artificial.
Este equipamento utiliza um software de processamento e interpretação de imagens que, combinado com um sistema de filtros e luz polarizada, permite avaliar dois aspectos importantes dos óvulos: a birrefringência da zona pelúcida e a presença e posição do fuso meiótico.
A análise da birrefringência da zona pelúcida permite observar a estrutura da camada externa que envolve o óvulo. Essa avaliação funciona como um marcador indireto da qualidade do oócito, ajudando a identificar óvulos com melhor potencial.
Já a avaliação do fuso meiótico possibilita identificar os óvulos com maior chance de fertilização e bom desenvolvimento embrionário. Além disso, pode indicar quando alguns óvulos apresentam maior risco de originar embriões com alterações cromossômicas.
Ambas as análises são consideradas não invasivas, pois não utilizam corantes ou substâncias que possam interferir nos óvulos. Dessa forma, preservam sua integridade e, consequentemente, a qualidade dos embriões.
Por isso, essas técnicas são ferramentas importantes na avaliação da qualidade dos óvulos, contribuindo para melhores decisões durante os tratamentos de fertilização in vitro (FIV).
A oncofertilidade é uma especialidade, que visa ajudar pacientes com câncer a manterem a sua fertilidade preservada, através de técnicas de Reprodução Assistida, para que no futuro, após tratamento da doença, possam ter a oportunidade de constituir família.
As opções terapêuticas de tratamento do câncer, são agressivas, podendo levar à infertilidade temporária ou permanente, seja pela remoção dos órgãos reprodutivos, através de abordagem cirúrgica, ou pela ação gonadotóxica da quimioterapia e radioterapia, sobre a função ovariana e testicular. Porém, graças a programas de rastreamento mais amplos, diagnósticos mais rápidos e estratégias terapêuticas mais eficazes, a taxa de sobrevida aumentou, levando os médicos a se concentrarem, também, em questões de qualidade de vida a longo prazo, incluindo o acesso à parentalidade.
A preservação do material biológico antes da realização dos tratamentos para o câncer possibilita que, no futuro, os pacientes tenham mais chances de constituir família, uma vez que a paternidade e maternidade são um grande sonho.
Na Clínica Conceber, temos uma equipe de especialistas capacitados, que oferecem aos pacientes opções para preservar a fertilidade.
Como é o Tratamento de Oncofertilidade?
Alguns aspectos a serem pontuados individualmente para trilhar o tratamento de preservação da fertilidade. Inicialmente, a paciente portadora de um diagnóstico de câncer está lutando contra o tempo, e nosso objetivo é iniciar imediatamente a abordagem para proporcionar o start do processo.
Através do nosso canal aberto de contato para oncofertilidade, a paciente pode tirar as suas dúvidas e agendar a sua primeira consulta já na mesma semana. Caso deseje, o início do processo poderá ocorrer no mesmo dia.
Para mulheres, em idade fértil, as opções terapêuticas são:
– Criopreservação de oócitos,
– Criopreservação de embriões
Para preservação da fertilidade masculina, temos:
– Criopreservação de espermatozóides;
A coleta de espermatozoides para criopreservação é indicada, seja por masturbação ou extração direta do testículo, através de processo microcirúrgico. Esses materiais são armazenados em nitrogênio líquido, a menos 196ºC, aguardando o momento para serem utilizados pelo paciente/casal.
Por que escolher o Tratamento de Oncofertilidade?
A oncofertilidade é responsável por trazer resultados satisfatórios e auxiliar que mulheres e homens em idade reprodutiva acometidos pelo câncer possam ter a oportunidade de tentar a gestação com seu próprio material genético.
Integrados, Oncologia e Reprodução Humana proporcionarão aos pacientes oncológicos, um sentimento de esperança, uma força a mais para lutar e chegar a um futuro cheio de possíveis realizações.
Os avanços na área da reprodução assistida foram, e ainda são responsáveis por tornar real o sonho da maternidade, da paternidade. No entanto, a sofisticação e modernidade dos procedimentos trouxeram muitos outros benefícios, inclusive na identificação de doenças ainda nos embriões por meio do PGT (teste genético pré-implantacional).
O PGT é caracterizado por uma análise de possíveis alterações cromossômicas e genéticas, que sinalizam doenças e condições de saúde, como a síndrome de Down, pode ser realizada em diferentes estágios de desenvolvimento dos embriões. Sendo assim, na etapa final da fertilização in vitro (FIV), que é a implantação uterina, são selecionados os embriões livres de alterações.
Além da síndrome de Down, o teste genético pré-implantacional pode idêntica previamente:
PGT-A E PGT-M
Para facilitar o entendimento, sobretudo dos pacientes, a comunidade médica padronizou os termos, portanto, o diagnóstico que visa investigar a presença de modificações cromossômicas e genéticas é chamado de teste genético pré-implantacional (PGT). Além dele, existem exames agregados, ou seja, que complementam o diagnóstico de acordo com a necessidade, caso, etc.
PGT-A: Neste teste complementar, que leva a sigla PGT seguido da letra A de aneuploidia, o objetivo é identificar a saúde dos cromossomos do embrião, portanto, a análise também compreende em reduzir o abortamento e doenças citadas acima, como a síndrome de Down. Quando existem quadros de aborto em repetição, o PGT-A também é indicado.
PGT-M: Neste outro teste complementar, que leva a sigla PGT seguido da letra M de monogênica, o objetivo é investigar se algum dos embriões que serão implantados apresentam alterações genéticas, principalmente quando há registro de doenças hereditárias na família, como por exemplo anemia falciforme, fibrose cística, Hemofilia, Distrofia Miotônica, Síndrome do X-Frágil, Distrofia Muscular, Doença de Huntington, entre outras no casal ou pessoa que vai passar pela fertilização in vitro (FIV). Portanto, PGT-M é uma avaliação que visa ajudar na escolha de embriões sadios, e desta forma, estabelecer que a gestação não seja afetada por possíveis mutações genéticas.
Atualmente, 86% das pessoas infectadas pelo vírus HIV estão em idade reprodutiva (entre 15 e 44 anos). Com a evolução da tecnologia, já é possível que homens ou mulheres HIV positivo tenham filhos.
Quando o portador do vírus é mulher, a solução é realizar a inseminação intrauterina, o que elimina a possibilidade de transmissão do vírus ao parceiro. Em relação ao bebê, a evolução até agora também foi grande: uma gestante sem tratamento tem uma taxa de transmissão do vírus para seu feto de 20-25%. Com abordagens avançadas durante a gestação e a amamentação este risco de transmissão do vírus reduz para menos de 1%.
Quando o portador é homem, o procedimento usado é separar espermatozoides do vírus HIV, através de avançadas técnicas laboratoriais, e o uso desses espermatozoides selecionados para inseminação dos óvulos, reduzindo de forma importante a possibilidade de transmissão do vírus à mulher.
A Incubadora Trigas é um equipamento utilizado no laboratório de fertilização in vitro (FIV) que reproduz, de forma mais fiel, às condições naturais do organismo feminino para o
desenvolvimento embrionário. Diferente das incubadoras convencionais, ela controla simultaneamente três gases: oxigênio, dióxido de carbono e nitrogênio, criando um ambiente mais estável e adequado para os embriões.
Esse controle permite reduzir o estresse celular e favorecer o desenvolvimento embrionário em condições mais próximas às encontradas no corpo humano. Além disso, a estabilidade do ambiente dentro da incubadora contribui para melhores condições de cultivo durante as fases iniciais do desenvolvimento do embrião.
Por isso, a Incubadora Trigas é uma tecnologia importante para otimizar o cultivo embrionário e auxiliar nos resultados dos tratamentos de fertilização in vitro.
A biópsia embrionária é um procedimento realizado durante o tratamento de fertilização in vitro (FIV), no qual algumas células do embrião são cuidadosamente retiradas para análise genética.
Essa técnica permite avaliar o material genético embrionário, auxiliando na identificação de possíveis alterações cromossômicas ou doenças genéticas. Com essas informações, é possível selecionar embriões com maior potencial de implantação e desenvolvimento saudável.
O procedimento é realizado por profissionais especializados e com equipamentos de alta precisão, preservando a viabilidade do embrião. Dessa forma, a biópsia embrionária contribui para tornar os tratamentos mais seguros e aumentar as chances de sucesso reprodutivo.
A VIOLET é a inteligência artificial (IA) da Future Fertility que fornece um relatório com as imagens dos seus óvulos e previsões personalizadas da probabilidade de cada um se tornar um embrião no quinto ou sexto dia (chamado blastocisto), com base em comparações com mais de 120.000 outras imagens de óvulos e seus resultados.
Os relatórios VIOLET utilizam um tipo de IA chamado Aprendizado Profundo (Deep Learning), que pode processar grandes quantidades de imagens para reconhecer padrões invisíveis ao olho humano. O software processa mais de 120.000 imagens de óvulos e os dados dos resultados de cada um em diferentes tipos de pacientes e regiões geográficas.
Quando novas imagens de oócitos são enviadas para o software Future Fertility pelo seu laboratório de fertilidade, a IA compara instantaneamente a nova imagem com todas as outras que já viu antes e fornece uma previsão da probabilidade do seu oócito apresentar resultados bem sucedidos.
Com base nessa análise, o VIOLET gera relatórios que auxiliam a equipe médica e embriológica a compreender melhor a qualidade dos óvulos obtidos em cada ciclo de tratamento. Essas informações podem contribuir para o planejamento de estratégias mais personalizadas durante a fertilização in vitro (FIV).
Ao fornecer dados adicionais sobre o potencial reprodutivo dos óvulos, o VIOLET ajuda a ampliar a compreensão sobre as chances de sucesso do tratamento e a orientar possíveis decisões em ciclos futuros.
O MAGENTA fornece imagens dos seus óvulos e pontuações personalizadas de qualidade dos óvulos com base em comparações com mais de 120.000 outras imagens de óvulos e seus resultados. Uma pontuação MAGENTA mais alta está correlacionada com uma maior probabilidade de seu óvulo se desenvolver em um embrião de cinco ou seis dias (chamado de blastocisto).
O relatório MAGENTA foi projetado para ser amigável ao paciente, capacitando você a ser um participante mais informado em sua jornada de fertilidade. Suas informações permitem que você tenha uma compreensão mais clara e personalizada de sua fertilidade, ajudando assim a melhorar seu planejamento futuro em consulta com seu médico.
Os relatórios Magenta utilizam um tipo de IA chamado Aprendizado Profundo (Deep Learning), que pode reconhecer padrões em vastas quantidades de imagens invisíveis ao olho humano. Nosso modelo foi construído utilizando mais de 120.000 imagens de óvulos e seus dados de resultados em diferentes tipos de pacientes e regiões geográficas.
Quando novas imagens de oócitos são carregadas no software Future Fertility pelo seu laboratório de fertilidade, a IA compara instantaneamente a nova imagem com todas as outras que ela viu antes e fornece uma pontuação de qualidade do óvulo (0-10) que está correlacionada com a probabilidade de seu óvulo se desenvolver em um blastocisto.
O Zymot é um dispositivo de seleção espermática utilizado no laboratório de reprodução assistida, especialmente em tratamentos de fertilização in vitro (FIV) e ICSI.
A tecnologia utiliza um sistema de microcanais que simula o percurso natural que os espermatozoides realizam no trato reprodutivo feminino. Nesse processo, apenas os
espermatozoides com melhor motilidade e maior integridade conseguem atravessar o dispositivo, permitindo uma seleção mais fisiológica.
Além disso, o método reduz a manipulação das células e dispensa etapas tradicionais de centrifugação, que podem gerar estresse celular. Dessa forma, o Zymot contribui para a seleção de espermatozoides com melhores características para serem utilizados nos procedimentos de fertilização.
O EmbryoGlue é um meio de cultivo desenvolvido exclusivamente para a transferência embrionária. Utilizado mundialmente, ele já foi aplicado em inúmeras transferências na Clínica Conceber, com excelentes resultados.
Esse meio aumenta a taxa de implantação do embrião, pois torna as células embrionárias mais semelhantes às células do endométrio, já que em sua composição há ácido hialurônico – substância também presente no útero.
É válido ressaltar que esse meio não possui contraindicações, podendo ser usado em transferências a fresco ou de embriões descongelados, tanto no terceiro quanto no quinto dia de desenvolvimento (blastocistos).

Diretor Técnico Médico:
Dr. Alessandro Schuffner
CRM 18822
Copyright © 2026 – Conceber Centro de Reprodução Humana Ltda – EPP | CNPJ: 07.729.132/0001-06 – Todos os Direitos Reservados.
Desenvolvido por Combustiva – A Agência de Comunicação Especialista em Medicina